
【疫学専門家監修】初心者のためのTTE:三つの時間軸とバイアス - ゼロから学ぶ因果推論 vol.3-2
2024.12.01
シリーズ紹介|ゼロから学ぶ因果推論
「医学研究は難しい」、きっと多くの方がそう感じているでしょう。
因果推論は、そんな複雑怪奇な医学研究にスッと一本の軸を通してくれる、まさに医学研究の原理原則とも言える学問です。
因果推論を学ぶことで、複雑に散らばっていた知識の断片が見事なまでに因果推論という幹へと体系立てられていきます。そしてきっと「論文、読めるようになってきたかも」、そんな気持ちになれるはず。
「ゼロから学ぶ因果推論」シリーズは、疫学専門家の監修のもとで「はじめて学ぶ人の気持ち」に寄り添い、具体例や図解を使用して「日本でいちばんわかりやすい因果推論の解説」を目指しました。あなたの歩幅で一歩ずつ。ゼロからの学びをはじめしょう。
はじめに
本記事では、昨今のデータ分析手法において非常に注目されているTarget Trial Emulation(TTE)について、医師がイラスト付きでわかりやすく紹介します!
以下の3パートに分けて解説していきます。
Part 1 :ETAFOCAフレームワークについて
Part 2 :三つの時点で考えるバイアスとその対処法
Part 3 :論文の実例で理解を深めるTTE
この記事はPart 2であり、「TTEの実施にあたり留意すべき三つの時間軸と陥りやすいバイアス」について解説していきます。
mMEDICI Library | ひらけ、叡智の扉
叡智の扉を、全ての人が開けるように——。
学びは、限られた豊かな人々だけの特権ではありません。
経済的困難に直面する人、地方で学習資源に恵まれない人、家事や育児・仕事に追われる人。
mMEDICI Libraryではそんな人々にこそ、最高の学びを届けるため、研究・キャリア・学習・受験のあらゆるテーマでパブリックヘルスの叡智を集めました。
隙間時間にスマホひとつで、誰もが「一流の知」に触れることを叶えていきます。
「ここを開けば、誰しもが悩みを解決できる」、そんなメディアを目指します。
- シリーズ紹介|ゼロから学ぶ因果推論
- はじめに
- mMEDICI Library | ひらけ、叡智の扉
- この記事のまとめ
- この記事を読むと分かること
- この記事は誰に向けて書いているか
- 因果推論シリーズ
- 執筆者の紹介
- 編集者
- 監修者
- RCT模倣のための鍵
- 三つの時間軸(Time-zero、治療割付、対象者選択)
- 治療割付・Time-zeroの後に対象者が選択されるパターン
- 治療割付とTime-zero(追跡開始)が一致しないパターン
- 治療割付の後にTime-zeroが来てしまうパターン(実際の治療割付と、設定した治療割付がズレるパターン)
- 治療割付の前にTime-zeroがきてしまうパターン
- 終わりに
- 参考文献
- 因果推論を学ぶならオンラインスクールmJOHNSNOW
- 【YouTubeラジオコンテンツ 耳から学ぶシリーズ】
この記事のまとめ
この記事を読むと分かること
観察研究のデザインを向上するためのフレームワークであるTarget Trial Emulationを包括的に分かりやすく学ぶ
この記事は誰に向けて書いているか
これから医療大規模データベースを用いた観察研究を行いたいと考えている方
因果推論の手法を学びたいと考えている方
Target Trial Emulationを学びたい、もしくは独学したが挫折してしまった方
因果推論シリーズ
vol.1:因果推論の出発点 - 因果と関連の違いとは? -
vol.2:因果効果の基本を徹底解説 - Individual Causal Effect(個人因果効果)とAverage Causal Effect(平均因果効果)の違いとは? -
vol.3:初心者のためのTarget Trial Emulation(TTE)
- Part 1 ; ETAFOCAフレームワークについて
- Part 2 ; 三つの時点で考えるバイアスとその対処法
- Part 3 ; 論文の実例で理解を深めるTTEvol.4:Exchangeability(交換可能性)を徹底解説 - Randomization(ランダム化)が実現する因果推論の必須条件 -
vol.5:Standardization(標準化)を徹底解説 - 交絡調整の基本をわかりやすく図解 -
vol.6:Inverse Probability Weighting(逆確率重み付け)を徹底解説 - 交絡調整の基本をわかりやすく図解 -
vol.7:Consistency(一致性)を徹底解説 - 観測データと反事実アウトカムを一致させよ -
vol.8:Positivity(正値性)を徹底解説 - 因果推論の落とし穴を回避せよ -
vol.9:Immortal time biasを徹底解説 - 臨床研究に潜む「不死の時間」の罠 -
vol.10:効果修飾を徹底解説 - 私たちは「どの集団における」効果を見ているのか? -
vol.11:交互作用を徹底解説 - 複数の介入による相乗効果 -
vol.12:DAGを徹底解説
vol.13:交絡を徹底解説 - 結果を歪める、因果推論の最重要課題 -
vol.14:選択バイアスを徹底解説 - 消えた患者が結果を歪める?-
執筆者の紹介
氏名:吉田拓人(Google scholarはこちら,Linkedinはこちら)
所属:岩見沢市立総合病院外科
経歴:外科専門医・内視鏡技術認定医・公衆衛生学修士・JDLA-E資格。2014年から一般外科医として8年間勤務した後、米国ハーバード公衆衛生大学院でMPH取得。卒業後はカナダのUniversity Health Networkで外科医療AIのリサーチフェローを修了し、2024/09より現職。専門は消化器癌およびヘルニア診療、内視鏡手術。外科医のスキル評価、合併症の低減のためのデータ分析・医療AI開発に取り組んでいる。
編集者
氏名:菊池祐介
所属:mMEDICI株式会社
専門性:作業療法学修士。首都大学東京(現東京都立大学)・東京都立大学大学院を卒業後、病院勤務を経て専門学校・私立大学にて作業療法教育、地域共生社会の醸成に向けたリハビリテーション専門職の支援に関する研究に従事。現在は心身の健康とその人らしさの実現に向け、保険内外でのクライアント支援を展開している。作業療法の社会的意義向上を信念に、mMEDICI株式会社に参画。
監修者
氏名:廣瀬直紀
所属:mMEDICI株式会社
専門性:保健学博士・公衆衛生学修士。東京大学・東京大学大学院を卒業後、外資系製薬企業の日本・グローバルにおいて疫学専門家として薬剤疫学・リアルワールドデータ研究に従事。その後、全ての人がアクセス可能な一流の知のプラットフォームを作り、「知に繁栄を、辺野に豊穣を」実現すべく、mMEDICI株式会社を創業。
RCT模倣のための鍵
三つの時間軸(Time-zero、治療割付、対象者選択)
Target Trial Emulationの研究デザインを考える上では、次の三つの時間軸が非常に大切になります。
・Time-zero
・治療割付
・対象者選択なんだそれは?
と思われたかもしれませんが、この後に定義をしっかり解説しますのでご安心ください。
RCTを適切に模倣するためには、これら三つの時間軸が重なるように設定する必要がありますが、観察データを用いた研究ではこの三つの時間軸がズレやすく、それにより様々なバイアスが発生することで頑健な因果効果の推定が難しくなってしまいます。
この記事では、この三つの時間軸の役割と、それぞれの関係性が因果推論の頑健性を左右するかについて詳しく解説したいと思います。
なお、本記事は以下の論文を下敷きにしながら執筆しました。
Hernán MA, Sauer BC, Hernández-Díaz S, Platt R, Shrier I. Specifying a target trial prevents immortal time bias and other self-inflicted injuries in observational analyses. J Clin Epidemiol. 2016 Nov;79:70-75. doi: 10.1016/j.jclinepi.2016.04.014. Epub 2016 May 27. PMID: 27237061; PMCID: PMC5124536.
また、同じくkrskさんのブログも参考にさせて頂いております。
さて、まずは三つの時間軸の言葉の定義から説明しましょう。
1)Time-zero (タイムゼロ)
Time-zeroはフォローアップの開始時点、つまり「いつから対象を追跡し始めるか」という時点です。Start of follow-upやBaselineとも呼ばれ、これは治療の開始時点と重なることが理想的です。
「治療が開始する1ヶ月前や、治療が開始して1ヶ月後からアウトカムの追跡を開始しました」と言われると「えっ?」という感覚になることに違和感はないかなと思います。
2)治療割付
治療割付とは、患者を治療群または対照群に振り分ける時点です。
RCTをイメージすると、ランダム化でそれぞれの患者が「どの治療を受けるか」が決定した時点です。
3)対象者選択
対象者選択は、研究に参加する患者を選択するタイミングです。
RCTでは対象者は治療割付前に選定されます。
理想的なRCTでは、対象者選択、治療割付、フォローアップ開始(=Time-zero)の三つの時間軸が以下の図のように一致します。
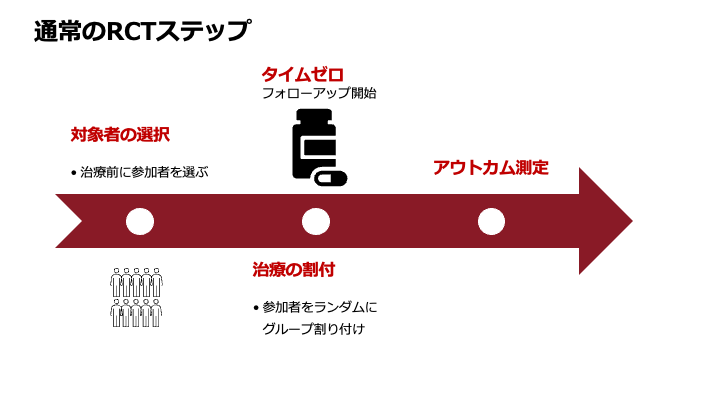
対象者を選択し、治療の割付を行い、そしてそれと同時にフォローアップを開始するというように。
しかし、観察研究では様々な外部要因によりこの三つの時間軸を揃えることが難しく、その結果として様々なバイアスが発生します。
それでは、外科医の視点から具体的に解説していきましょう。
治療割付・Time-zeroの後に対象者が選択されるパターン
観察研究では、以下のような状態が生じてRCTを模倣できないパターンが起こり得ます。
RCT:まず対象者を選択し、その後に治療を割付、Time-zeroから追跡を開始する
観察研究:治療に曝露した患者を見つけ、曝露時点から追跡を開始するが、途中で治療を中断したり、そもそもデータが測定できなくなってしまった患者を除いて解析を行う(つまり、治療割付・Time-zeroの後に最終的に対象患者を選択している)
大腸癌術の補助化学療法を例にして具体的に考えてみます。
リサーチクエスチョン:大腸癌術後の補助化学療法は、それを行わなかった場合と比較して生存率を向上し、再発率を低下させるか?
このリサーチクエスチョンにおいて、最後まで追跡できた患者だけで解析を行う、つまり「治療割付・Time-zeroよりも後に対象者選択をする」と何が起こるでしょうか?
視覚的にわかりやすくするために、まず上記の状態をDAGにしましょう。

【A→C】
補助化学療法を受けた患者は、その副作用によって途中で治療を中断し、追跡から脱落しやすくなる【L→C】
合併症がある患者は体調の問題で追跡から脱落しやすい【L→Y】
合併症がある患者は、体調が悪いため生存率が低く、再発率が高いさて、この三つの条件が揃った際に、脱落せずに最後まで追跡できた患者だけで解析を行うとどのようなバイアスが生じるでしょうか?
少しややこしいのですが、以下のようなバイアスが生じます(ぜひゆっくりと咀嚼してみてください)。
脱落せずに最後まで治療を補助化学療法を続けられた患者は、「副作用によって脱落する可能性が高いにも関わらず(A→C)」、脱落が起こらないほど元々の体調が良かった患者(L→C)であった、と言うことができます。
そして、これらの患者は「もともとの体調が良かったため、生存率が高く、再発率が低い」患者です。
つまり、補助化学療法を受けた患者を「最後まで補助化学療法を続けられた患者」に限定すると、彼らの中には「それだけ元々の体調が良かった患者」が多く存在し、よって治療成績が向上する方にゲタが履かせられている、と言えるでしょう。
このようなバイアスを「選択バイアス」と呼びます。
「最後まで脱落せずに補助化学療法を続けられた患者」だけを”選択”することで起こるバイアスだから、「選択バイアス」ですね。
疫学研究に触れたことがある方は「脱落した患者を除外するのは研究デザインとして望ましくない」という話を聞いたことがあるかもしれませんが、それはこの「選択バイアス」が生じる可能性があるからです。
ちなみに形式ばった表現をすると、この選択バイアスは以下の条件が揃うと発生します。
割付られた治療によって脱落の確率が影響される
脱落した人としなかった人でアウトカムの予測因子の分布が異なる
ですので、「脱落者がいれば必ず選択バイアスが発生する」と単一的に判断するのではなく、そんな時も「この脱落を解析から除外してしまうと、選択バイアスは発生するだろうか?」と冷静に考えることが大切になります。
治療割付とTime-zero(追跡開始)が一致しないパターン
治療割付の後にTime-zeroが来てしまうパターン(実際の治療割付と、設定した治療割付がズレるパターン)
「どんなパターンだそれは」という声が聞こえてきそうですが、例えばこれは「実際に治療割付をしたタイミングが分からないので、とりあえず”この時点からにしよう”として治療割付の時点を決める」際などに生じます。
RCT:まず対象者を選択し、その後に治療を割付、そしてそれと同時にTime-zeroから追跡を開始する
観察研究:患者を包含したが、過去のデータが限定的のためいつから治療を受けているかわからない。そのため実際の治療割付よりも後の時点を”仮の治療割付”として、そこにTime-zeroを設定して追跡を開始する

具体的に考えるため、術前の貧血と鉄剤投与の効果評価について考えてみましょう。
リサーチクエスチョン:貧血患者における外科手術における術前の鉄剤の投与は、投与しなかった時と比べて術後アウトカムを改善させるか?
外科手術を受ける患者において、術前の貧血は手術後の合併症リスクを高め、回復を遅らせる要因とされています。そのために、術前に鉄剤を投与して貧血を改善することで、手術後のアウトカムが改善する可能性があります。
ある研究者が、術前の鉄剤投与が手術後の合併症発生率や回復速度に与えている効果を評価したいと考えています。
そこで、鉄剤を投与されている貧血患者と投与されていない貧血患者を比較し、その後のアウトカムを追跡しようとしたとします。
この研究を行うため、各施設から集められるレセプトで構成させるレセプトデータベースを証することにしました。
術前の入院時点での鉄剤の使用状況をもって治療割付を判断することにしましたが、ここで一つ問題が起こります。
今回使用するデータベースは入院中のデータしかないため、入院時点で鉄剤を使用していた患者が、「実際はいつから鉄剤を使用していたか(治療割付)」が不明なのです。
つまり、実際の治療割付と設定した治療割付(入院時点)がズレてしまう可能性があります。
さて、このような状況ではどのようなバイアスが生じるでしょうか?
視覚的に分かりやすくするために今回もDAGを活用しましょう。
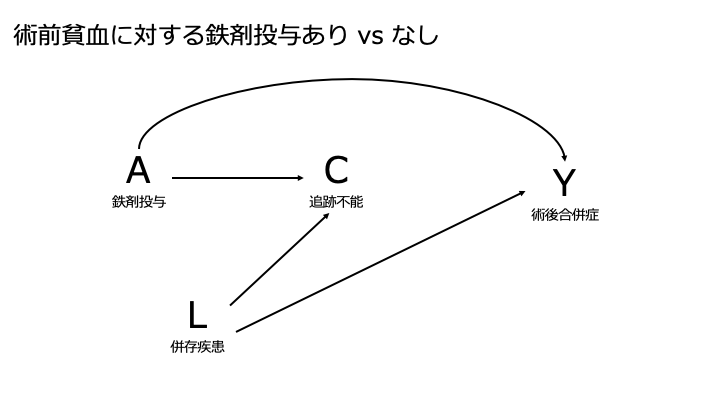
【A→C】
鉄剤投与を受けた患者は、副作用によって鉄剤の内服を中断しやすい【L→C】
併存疾患がある患者は体調の問題で追跡から脱落しやすい【L→Y】
併存疾患がある患者は術後合併症を起こしやすい今回「鉄剤あり」を割付られた患者は(観察研究なので実際にRCTのように割り付けを行っているわけではありませんが)、「入院時点まで中断せずに鉄剤を使い続けた患者」になります。
つまりここでも患者の「選択」が起きていますね。
ここまで読んだみなさんは「もしや」とピンときているでしょう。
そう、選択バイアスです。
鉄剤を使うと副作用で脱落しやすいにも関わらず、鉄剤を使い続けられた患者は、それだけ併存疾患が軽症であった可能性があります。そして、併存疾患が軽症ということは、彼らは術後合併症のリスクが低い患者です。
このように「鉄剤を使い続けられた患者」だけに限定して解析を行うと、鉄剤あり群は術後合併症リスクが低い患者が集まり、下駄を履かせられた状態になるわけです。
なお、薬剤疫学の世界ではこのような患者をPrevalent user(既存使用者)と呼び、これにより生じる選択バイアスをPrevalent user biasと呼びます。
Prevalent user biasを回避する方法としては、既存使用者ではなくTime-zeroにおいて新規に薬剤を使用し始めたNew userだけに限定するという手法があり、この研究デザインをNew user designと呼びます。
治療割付の前にTime-zeroがきてしまうパターン
Time-zeroが治療割付よりも前、つまり治療を割り付けるよりも前から患者の追跡をするパターンです。
「治療の効果を見たいのに、その割り付け前から患者を追跡するはずがないだろう」と思うかもしれませんが、この失敗によって痛い目を見ている研究も実際に存在します。
RCT:まず対象者を選択し、その後に治療を割付、Time-zeroから追跡を開始する
観察研究:患者を包含してから、ある条件を満たした段階で曝露群とする。しかし、Time-zeroをその条件を満たした段階(つまり治療割付)ではなく、それよりも前の時点に設定してしまう

例えば、外科手術後のICU滞在期間が術後の合併症リスクに与える影響を調査する場合を想定してみましょう。
リサーチクエスチョン:外科手術後のICU滞在期間が1週間以上の患者は、それ未満の患者と比較して術後合併症リスクが高いか?
ある研究者が、「ICUに1週間以上滞在した患者」と「1週間未満滞在した患者」で術後の合併症リスクを比較したとします。
下記の図に示すように、理論的には死亡した患者は以下の三つに分けられます。

患者A:ICUの滞在期間が1週間未満で、1週間以降に死亡した患者
患者B:ICUの滞在期間が1週間未満で、1週間未満に死亡した患者
患者C:ICUに1週間以上滞在し、死亡した患者
の三つになります。
さて、この時にTime-zero、つまりアウトカムの追跡を開始する時点はどこに設定すべきでしょうか?
本来であれば、「治療割付と同時」にTime-zeroを設定しなければなりませんから、以下のようになります。
ICU滞在期間が1週間未満の患者:ICU入室時
ICU滞在期間が1週間以上の患者:ICU入室1週間時点
しかし、ここで誤って以下のようにTime-zeroを設定してしまったとしましょう。
ICU滞在期間が1週間未満の患者:ICU入室時
ICU滞在期間が1週間以上の患者:ICU入室時
ご覧の通り、2番の患者も「ICU入室時」から追跡を開始しています。
こう説明すると「ICU1週間入院の影響を測るのに、1週間入院する前からアウトカムを追跡するのはおかしい」と気づけるかもしれません。
説明なしに「Time-zeroをどこに設定しますか?」と問題を出されるとついつい「ICU入室の影響を測定するんだから、ICU入室時点でしょ」と答えてしまう気持ちもわかりますね。
さて、これはつまり治療割付の前にTime-zeroを設定してしまっているパターンです。
この時、どのようなバイアスが生じるでしょうか?
ICU滞在期間が1週間以上の群に割り振られた患者は、必然的にICU入室から1週間は生存することが決定しています。
なぜなら、1週間以内に死亡してしまった場合は自動的に「ICU入室が1週間未満の患者」に割り振られてしまうからです。
とすると、「ICU滞在期間が1週間以上の患者」では、アウトカムにおいて「絶対に死なない1週間」がボーナスとして自動で付与されることになります。
これにより、1週間分だけ見かけ上のアウトカムが改善したようにみえてしまうバイアスが生じます。
この1週間の絶対に死亡が発生しない時間をImmortal time(不死時間)と呼び、そしてこれにより生じるバイアスをImmortal time biasと呼びます。
このように治療割付のタイミングが決まるのがTime-zeroよりも後の場合は、このImmortal time biasに注意する必要があります。
Immortal time biasの詳細はコチラの記事で解説
「そんなミスするわけないだろう」と思った方もいらっしゃるかもしれません。
ではここで、このImmortal time biasが問題になった例があるので紹介しましょう。
Immortal time biasが過去に起こった例
1.パキロピッドはCOVID-19感染後の入院リスクを下げるか?[1]
こちらは2023年に、The Lancet Infectious Diseaseから報告された論文ですが、Immortal time biasがとりわけ大きく注目された論文になります。
本論文で用いられた研究デザインの概要は下記の通りです。
P:COVID-19感染後、非入院で治療を受ける成人患者
I:パキロピッド治療群
C:パキロピッド非治療群
O:28日以内の全原因による死亡率
この研究デザインから導かれた結論は、パキロピッドが28日死亡率を下げる可能性があるというものでしたが、Immortal time biasが後に指摘されています。
その原因は、パキロビット治療群のTime-zeroをパキロビット投与時点ではなく、Covid-19感染時点としてしまったことでした。
パキロビット治療群は「パキロビットを投与されるまで死亡しなかった患者」ですから、Covid-19感染からパキロビット治療開始までにはImmortal timeが発生します。
タイムゼロをCovid-19感染時点としたことでこのImmortal timeの分だけパキロビット治療群は効果に下駄を履かせられたことになり、見かけ上の治療成績が良くなったのです。
2.喘息増悪で入院した患者に対する抗菌薬治療が入院期間及ぼす影響は?[2]
この論文のリサーチクエスチョンは、喘息増悪で入院しステロイド治療を受ける患者において、抗菌薬治療は入院期間に影響を与えるか?というものです。
研究デザインは以下の通りです。
P:喘息増悪のため入院し、コルチコステロイド投与を受ける患者
I:入院2日以内に抗菌薬治療を開始し、少なくとも2日間投与された患者
C:抗菌薬治療を受けなかった、または3日目以降に開始した患者
O:入院期間
この研究デザインから導かれた結論は、抗菌薬治療群は非治療群に比較して入院期間が有意に長く(中央値で1日長い)、入院コストが高いというものでした。
しかし、後に読者からImmortal time biasが生じていることを指摘されています。
その原因は、治療群に「抗菌薬を2日以上投与されること」という条件を設けた点です。この条件のため、治療群は2日以上入院することが必須となり、その期間がImmortal timeとなることで治療群の見かけ上の治療成績が悪くなったのです。
なお、この論文の筆者らはこの指摘を受け一度論文を撤回し、再度下記のようなデザインで解析をし直しています。
P:喘息増悪のため入院し、コルチコステロイド投与を受ける患者
I:入院1日目に抗菌薬治療を開始した患者(2日間投与の条件を撤廃)
C:抗菌薬治療を受けなかった、または2日目以降に開始した患者
O:入院期間
このように抗菌薬治療開始日を1日目に限定し、2日以上の投与条件を排除することで、Immortal time biasを回避しました。
新たなデザインでの解析の結果、抗菌薬治療群では入院期間の延長は統計的には有意でしたが、その差は臨床的には意味がないものでした(中央値でわずか0.11日の差)。
このような論文に対するやり取り、撤回から再投稿に至るプロセスは、科学者としてあるべき姿を学ぶようにも思います。
終わりに
いかがでしたでしょうか?
観察研究を行う上で、Time-zero・治療割付・対象者選択という三つの時間軸を正しく扱うことの大切さがご理解いただけたかと思います。
さて、TTEシリーズ最終回となるPart 3では、より具体的にTTEを理解するため実際にTTEが用いられた論文を幾つかご紹介したいと思います!
参考文献
ウェブサイト
UNBOUNDEDLY (https://www.krsk-phs.com/entry/target.trial)
全てのものは、毒であり(https://nothing-without-poison.com/epi3/)
ハーバード流 リアルワールドデータ徹底活用講座〜RCTを模倣し、落とし穴を回避セヨ〜 Target Trial Emulationという僕らの新たな武器について(https://merasmus-r-20240727.peatix.com/view)
参考文献
Aggarwal, N. R. et al. Real-world use of nirmatrelvir-ritonavir in outpatients with COVID-19 during the era of omicron variants including BA.4 and BA.5 in Colorado, USA: a retrospective cohort study. Lancet Infect. Dis. 23, 696–705 (2023).
Stefan, M. S. et al. Association of antibiotic treatment with outcomes in patients hospitalized for an asthma exacerbation treated with systemic corticosteroids. JAMA Intern. Med. 179, 333–339 (2019).
参考図書:『Causal Inference: What If』
Causal Inference: What Ifとはハーバード大学のSPHで教鞭をとるMiguel Hernan氏とJames Robins氏によって執筆された因果推論の金字塔的書籍です。
mJOHNSNOWでは、こちらの書籍を用いて輪読会を行い因果推論をゼロから学んでいます。
因果推論を学ぶならオンラインスクールmJOHNSNOW

この記事を読み、「もっと因果推論を学びたい」と思われた方もいらっしゃるでしょう。
そんな方には弊社が運営するオンラインスクールmJOHNSNOWがお勧めです。mJOHNSNOWはスペシャリストが運営する臨床研究・パブリックヘルスに特化した日本最大規模の入会審査制オンラインスクールです。運営・フェローの専門は疫学、生物統計学、リアルワールドデータ、臨床、企業など多岐に渡り、東大、京大、ハーバード、ジョンズホプキンス、LSHTMなど世界のトップスクールの卒業生も集まっています。
本日解説した因果推論の講義に加えて、みなさんの専門性を伸ばすためのコンテンツが目白押しです!
・スペシャリスト監修の臨床研究・パブリックヘルスの講義が毎月7つ以上開催
・過去の講義が全てオンデマンド動画化されたレポジトリー
・スクール内のスペシャリストに学術・キャリアの相談ができるチャットコンサル
・フェローが自由に設立して学べるピアグループ(ex. RWDピア)
・24時間利用可能なオンライン自習室「パブリックヘルスを、生き様に」をミッションに、『初心者が、自立して臨床研究・パブリックヘルスの実践者になる』ことを目指して学んでいます。初心者の方も大勢所属しており、次のような手厚いサポートがあるので安心してご参加ください!
・オンデマンド動画があるから納得するまで何回でも、いつでも学び直せる
・チャットコンサルで質問すれば24時間以内にスペシャリストから複数の回答が
・初心者専用の「優しいピアグループ」で助け合い、スペシャリストが”講義の解説”講義を毎月開催【YouTubeラジオコンテンツ 耳から学ぶシリーズ】

YouTubeラジオコンテンツ「耳から学ぶシリーズ」は、仕事や育児で忙しい人が10分のスキマ時間に“ながら聞き”で学べる音声コンテンツです。
すべてのコンテンツを疫学専門家が監修し、完全無料で毎日投稿していきますので、ぜひチャンネル登録してお待ちください。
シリーズ一覧
因果推論シリーズ
vol.1:因果推論の出発点 - 因果と関連の違いとは? -
vol.2:因果効果の基本を徹底解説 - Individual Causal Effect(個人因果効果)とAverage Causal Effect(平均因果効果)の違いとは? -
vol.3:初心者のためのTarget Trial Emulation(TTE)
- Part 1 ; ETAFOCAフレームワークについて
- Part 2 ; 三つの時点で考えるバイアスとその対処法
- Part 3 ; 論文の実例で理解を深めるTTEvol.4:Exchangeability(交換可能性)を徹底解説 - Randomization(ランダム化)が実現する因果推論の必須条件 -
vol.5:Standardization(標準化)を徹底解説 - 交絡調整の基本をわかりやすく図解 -
vol.6:Inverse Probability Weighting(逆確率重み付け)を徹底解説 - 交絡調整の基本をわかりやすく図解 -
vol.7:Consistency(一致性)を徹底解説 - 観測データと反事実アウトカムを一致させよ -
vol.8:Positivity(正値性)を徹底解説 - 因果推論の落とし穴を回避せよ -
vol.9:Immortal time biasを徹底解説 - 臨床研究に潜む「不死の時間」の罠 -
vol.10:効果修飾を徹底解説 - 私たちは「どの集団における」効果を見ているのか? -
vol.11:交互作用を徹底解説 - 複数の介入による相乗効果 -
vol.12:DAGを徹底解説
vol.13:交絡を徹底解説 - 結果を歪める、因果推論の最重要課題 -
vol.14:選択バイアスを徹底解説 - 消えた患者が結果を歪める?-
©mMEDICI Inc. ALL RIGHTS RESERVED.










